近半年,上海交通大学生物医学工程学院古宏晨/徐宏课题组(纳米诊疗创新团队)在分析化学与生物传感领域知名期刊Biosensors & Bioelectronics、Sensors and Actuators: B. Chemical、ACS Sensors上连续发表多篇“编码微球-液滴”基多重数字式超灵敏生物检测研究成果。
研究背景
与疾病发生发展密切相关的低丰度生物标志物的超灵敏、多指标检测是生物医学领域的重大需求,但目前常用的检测技术往往无法在单管检测中同时实现多重生物标志物的精准鉴别和高灵敏检测。新兴的基于隔离分区模式的数字式生物检测平台虽能达到超高的检测灵敏度,但受限于荧光检测通道的数量与鉴别目标分子的编码方式,无论是核酸样本还是蛋白样本,单管反应中检测的目标分子种类均不超过10重。因此,如何在单管多重指标鉴别的同时实现超高灵敏检测是目前生物检测领域中极具挑战的瓶颈问题。
针对上述亟待突破的关键问题,古宏晨/徐宏团队聚焦可快速生成无限量分区的高通量液滴微流控平台,采用团队独创的编码微球载体,构建了新型“编码微球-液滴”基微流控芯片,并在此基础上发展了“蛋白-核酸”通用型超灵敏数字式生物检测技术。创新地实现了:(1)单个液滴对单个编码微球的装载率突破传统“泊松分布”的限制,极大提高了数字式生物检测的分析效率与检测通量;(2)多重蛋白和核酸分子在编码微球载体表面的单分子高效捕获、“单微球-单分子”待检编码信号的准确鉴别、单分子靶标信号放大与单分子检测。
主要内容
01 高效单编码微球封装的液滴微流控系统
在传统的液滴分区中,利用荧光编码微球作为鉴别、捕获靶分子的载体,虽可大幅提高检测重数与通量,但受限于泊松分布,液滴分区对单个微球的封装完全随机,通常仅有10%以下的分区为含有1个编码微球的有效液滴,90%的液滴为未封装编码微球的空液滴。这些冗余的空液滴会在后续的检测分析中造成分析资源的大量浪费。因此,基于“编码微球-液滴”的多重数字式检测方法学需要解决的首要问题是如何突破泊松分布的限制,让有且仅有一个编码微球的液滴分区比例大幅提高。针对此问题,该团队提出了一种集微球排列、液滴生成与微球包裹的集成式“编码微球-液滴”微流控芯片(bead ordered arrangement droplet system, BOAD)系统。首先利用巧妙的流体结构设计,在短至1 cm的微流道中实现微球的快速有序排列,进而将有序排列的微球一一封装入液滴。研究结果显示,BOAD系统可将包裹有单个编码微球的液滴分区比例大幅提升至86%,单个微球的封装效率是常规检测体系的9倍。进一步地,该研究还展示了54重编码微球的高效包裹与精准解码。最后,采用IL-10为模式待测分子,证明了构建的BOAD系统可实现超灵敏的数字式检测,检测灵敏度较传统流式免疫荧光提高500倍。上述结果均展示了BOAD系统在多重数字式超敏检测与单细胞分析等领域的强大应用潜力。
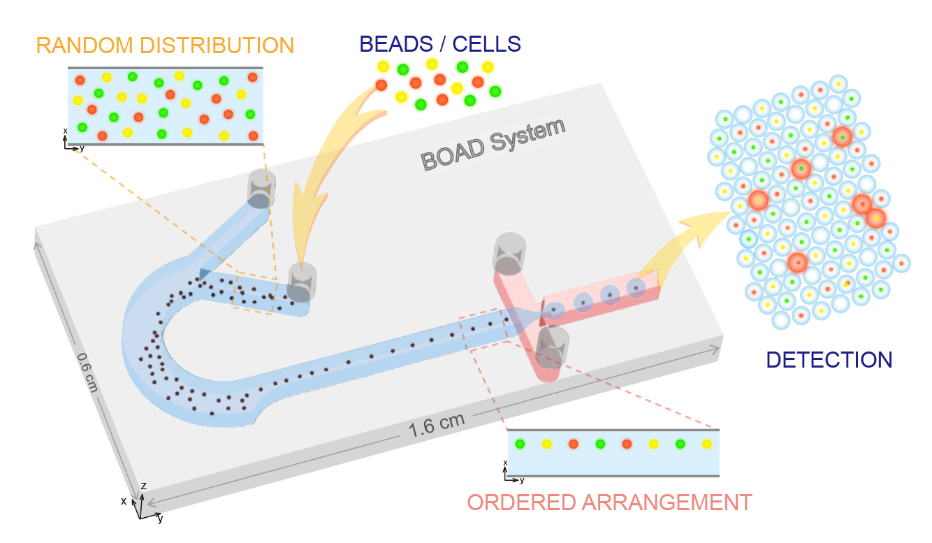
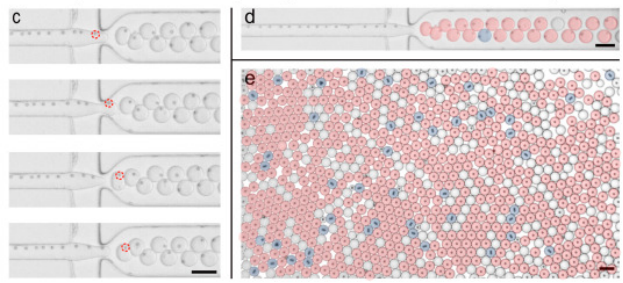
图1 课题组提出的高效单微球封装的液滴微流控系统
论文信息:
Xiaoyu Yue, Xiaoxia Fang*, Tong Sun, Jingwei Yi, Xiaojun Kuang, Qingsheng Guo, Yao Wang, Hongchen Gu, Hong Xu*. Breaking through the Poisson Distribution: A compact high-efficiency droplet microfluidic system for single-bead encapsulation and digital immunoassay detection. Biosensors and Bioelectronics, 2022, 211, 114384.
论文链接:
https://doi.org/10.1016/j.bios.2022.114384
02 “编码微球-液滴”基多重数字ELISA超敏检测系统
灵敏度到亚fM级别(fg/mL)的超灵敏、多重数字酶联免疫吸附(enzyme linked immunosorbent assay, ELISA)检测技术在基础生命科学研究和临床应用等方面(如肿瘤早筛、阿尔兹海默病血液基标志物的检测等)都具有重要的意义。该团队基于液滴微流控平台,以自主设计开发的新型荧光编码微球作为识别不同蛋白分子的载体,创新性地开发了一种兼具通用性与实用性的多重数字ELISA技术。首先,针对如何在直径几十微米的pL级液滴中实现直径仅几微米的编码微球精准解码难题,团队提出采用短、长曝光时间的二次成像方法,显著提高编码微球在液滴中的解码精度,为超高重蛋白分子的多重数字式检测提供可靠的检测平台。其次,针对pL液滴的单分子信号准确、快速检出问题,采用酶信号放大单元作为酶标记物,快速实现单个待测分子的信号放大,仅需5 min即可实现“1”和“0”液滴的区分与准确计数,显著缩短检测时间。最后,以TNF-α、IL-6、IFN-γ、IL-17A、IL-10等5种细胞因子为模式待测分子,在构建的“编码微球-液滴”微流控芯片上成功实现了单管多重蛋白的数字式检测,检测灵敏度较传统的多重悬浮芯片技术提升了100+~10,000+倍。该工作证明了“编码微球-液滴”基微流控技术有望成为临床超敏蛋白检测新的解决方案。
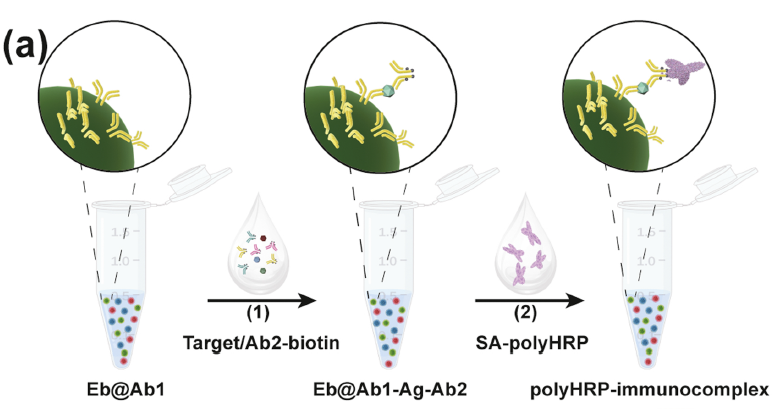
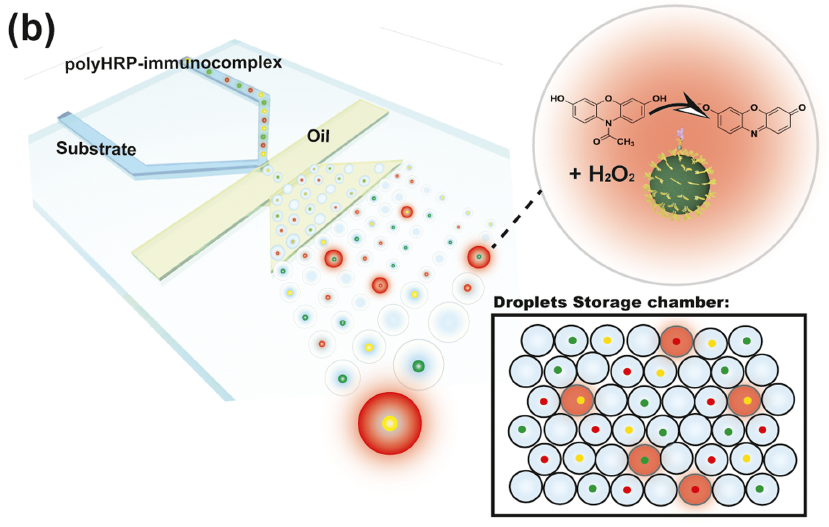

图2 “编码微球-液滴”基多重数字ELISA超敏检测系统
论文信息:
Jingwei Yi, Zehang Gao, Qingsheng Guo, You Wu, Tong Sun, Yao Wang, Hongbo Zhou, Hongchen Gu, Jianlong Zhao, Hong Xu*. Multiplexed digital ELISA in picoliter droplets based on enzyme signal amplification block and precisely decoding strategy: A universal and practical biodetection platform. Sensors and Actuators: B. Chemical, 2022, 369, 132214.
论文链接:
https://doi.org/10.1016/j.snb.2022.132214
03 “编码微球-液滴”基多重数字PCR检测系统
多重数字聚合酶链式反应(polymerase chain reaction, PCR)受到临床应用与基础生命科学研究等领域的日益关注。然而,当前的多重数字PCR技术缺乏兼具高灵敏度、高信噪比和超高多重靶标同时检测的有效策略。基于此,该团队提出了一种基于荧光编码微球的液滴基多重数字PCR超敏检测方法(Bead-based multiplexed droplet digital PCR)。该方法采用团队自主研发的超高编码容量荧光编码微球作为不同核酸的鉴别载体,从而大幅提升检测重数;进而结合通用引物与通用探针序列的巧妙设计,在“编码微球-液滴”微流控平台上实现高信噪比、超灵敏的多重核酸检测。在该方法中,以新型冠状病毒相关的orf1ab和N基因、甲型流感、乙型流感各自保守区基因以及阳控质粒作为模式待测靶标,通过预富集在不同靶基因上分别引入完全相同的通用序列;再利用固定有特异性探针的荧光编码微球,对富集后的不同核酸分子进行单分子特异性捕获,形成“单个编码微球-单个核酸分子”杂交复合物;最后,将上述微球杂交复合物包裹进含有通用扩增引物和通用荧光水解探针的液滴中,进行单反应多重数字PCR检测。该方法在流感病毒和新型冠状病毒的五重联检中可实现接近单分子级别的检测灵敏度,信噪比高且无交叉反应,为超高重数和超灵敏度的多重数字PCR技术奠定了基础,具有实际临床应用的潜力。

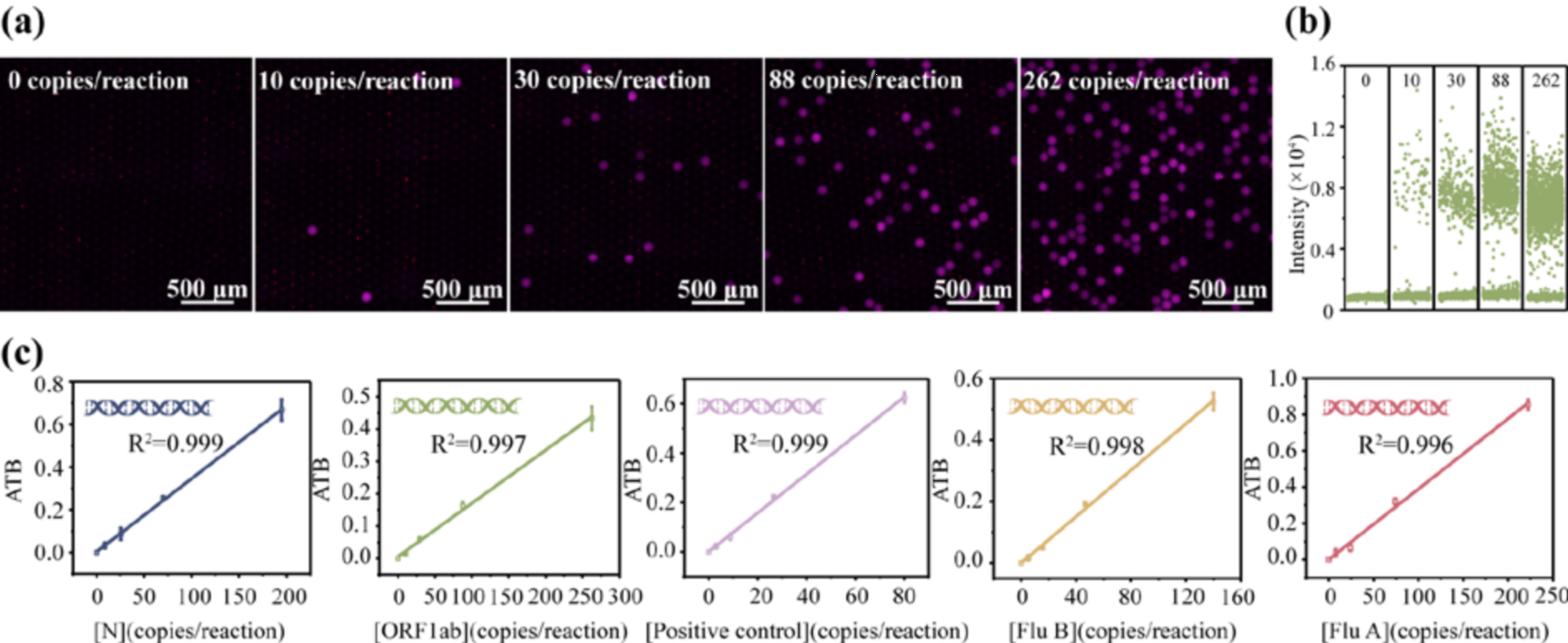
图3 “编码微球-液滴”基多重数字PCR检测系统
论文题目:
Zhejia Gu, Tong Sun, Qingsheng Guo, Yao Wang, Yunfei Ge, Hongchen Gu, Gaolian Xu*, Hong Xu*. Bead-based multiplexed droplet digital PCR in a single tube using universal sequences: an ultrasensitive, cross-reaction free, and high-throughput strategy, ACS Sensors, 2022-08-18 (accepted).
论文链接:
https://doi.org/10.1021/acssensors.2c01415
课题组简介:上海交通大学生物医学工程学院纳米诊疗团队(古宏晨-徐宏团队)以创新微纳材料与微纳技术为基础,秉承以解决临床问题为导向的科研理念,聚焦于纳米功能复合材料可控制备、生物检测创新方法、生物检测装备及系统、以及肿瘤新生抗原免疫治疗等研究方向。