近年来,一系列包含氰基、炔基以及氘原子等特殊基团的药物小分子被广泛研究,在DrugBank已收录的2327个上市药物分子中,约有2.4%的分子包含上述基团,如艾司西酞普兰、维拉帕米、利匹韦林、特立氟胺、维格列汀、托法替尼等。这些基团可以有效地提升药物分子的生物利用度、选择性、与靶蛋白亲和性和代谢稳定性。在药物的研发与筛选过程中,药代动力学特性至关重要,有助于了解药物的动态疗效以及更准确、及时地调整个性化治疗的用药剂量。目前的药代动力学检测通常通过液相色谱-质谱联用技术或高效液相色谱-质谱联用技术实现,但这些方法由于价格高、仪器设备复杂、预处理流程繁琐、操作专业要求高等因素,在临床普及、现场检测等的应用中受限。
表面增强拉曼光谱(Surface-enhanced Raman spectroscopy, SERS)是一种指纹式的振动光谱,基于无标记检测策略,可以根据谱峰特征实现包括药物分子在内的各种分子的检测,并且在SERS纳米颗粒表面的热点区域甚至可以达到单个分子的检测灵敏度,有利于微量药物分子的检测。此外,SERS检测所需要的仪器相对小型便捷、预处理流程简单、测试速度快,有利于在临床和基础研究中得到更加广泛和有效的应用。然而目前的SERS技术仍然面临着低浓度定量重复性差和生物体系背景干扰严重等的瓶颈问题,制约了其在真实生物样本和活体动物中的可用性。因此,目前亟需开发快速便捷、准确灵敏、可普遍推广的SERS技术用于药代动力学监测。
工作介绍
上海交通大学生物医学工程学院叶坚教授团队近期报道了基于单分子计数的数字胶体增强拉曼光谱技术(digital colloid-enhanced Raman spectroscopy, dCERS)(Nature, 2024, 628, 771-775),实现了超低浓度目标分子具有可重复性的定量能力。而在本研究工作中着重针对具有氰基、炔基以及氘原子等特殊基团的药物分子,结合数字胶体增强拉曼光谱技术,实现了活体动物的药代动力学监测。药物分子中的氰基、炔基以及氘原子等基团可以产生生物静默区(1800-2800 cm-1)的拉曼信号,有效避免了复杂生物分子体系在拉曼光谱指纹区(500-1800 cm-1)的信号混叠问题,提升药物分子信号读取的可靠性与灵敏度,这类分子也由此称为生物正交分子。此外,结合一步法血清预处理方案,减少了血清中蛋白等大分子对于SERS纳米颗粒表面热点区域的竞争作用,进一步提升了药物分子的检测灵敏度与可靠性(图1)。
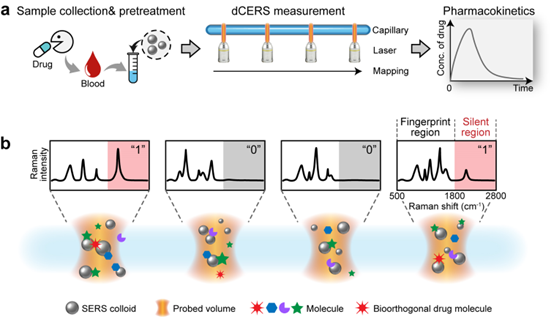
图1. 数字胶体增强拉曼光谱用于药代动力学监测的概念示意图
本文中,研究者选取了厄洛替尼作为目标药物分子。厄洛替尼是第一代表皮生长因子受体酪氨酸激酶抑制剂,常用于非小细胞肺癌的治疗,由于其具有末端炔基,可以产生位于拉曼光谱静默区的特征峰信号1982 cm-1,由此从谱峰特征复杂的血清光谱中可以准确识别厄洛替尼分子信号的有无,即判断当前光谱为阳性光谱或阴性光谱。
值得注意的是,真实生物样本中,由于大量不同种类的分子的存在,适当的预处理步骤有助于提高目标分子的检测能力。针对血清体系,研究者采用了乙腈作为蛋白沉淀剂来去除血清中大量存在的蛋白分子,防止了样本与纳米颗粒混合后颗粒表面蛋白冠的形成,从而使目标分子得以进入SERS纳米颗粒表面的热点区域。如图2所示,该一步预处理方法可以有效提升血清体系中厄洛替尼分子的检出率。
随后,根据厄洛替尼在静默区的特征峰,采用数字胶体增强拉曼光谱技术,基于厄洛替尼阳性光谱占样本内总检测光谱的比值建立了血清体系中厄洛替尼的定量标准曲线。由于该方法基于计数原理,定量误差符合泊松噪声,通过累计阳性光谱数量实现了定量重复性的精准调控。
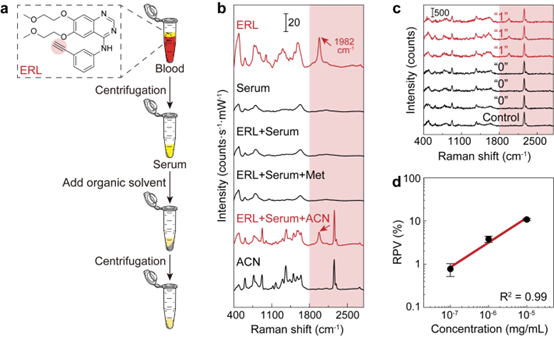
图2. 血清样本的预处理提升分子检出率以及基于静默区信号眼里建立血清中厄洛替尼数字化定量标准曲线
为了展现活体动物血液中厄洛替尼的药代动力学监测,研究者对雄性Wistar大鼠进行厄洛替尼灌胃给药,在给药后0至48小时的一系列时间点进行采血,根据标准方案从全血中获得血清,对血清预处理后进行SERS检测,计算每个样本所测得的光谱集内阳性光谱的比例,根据上述建立的定量标准曲线获得每一时刻血液中厄洛替尼的浓度,最终获得大鼠药代动力学曲线(图3),与液相色谱-串联质谱实验验证结果以及相关文献报道结果相一致,进一步说明了本文药代动力学监测方法的准确性与可靠性。
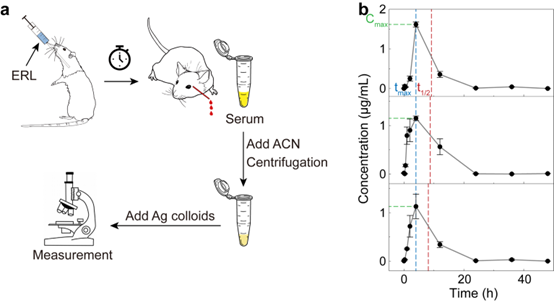
图3. 大鼠血液厄洛替尼药代动力学监测
综上所述,本工作开发了一种针对生物正交药物分子的药代动力学监测技术,基于静默区信号可以实现复杂生物体系中可靠的药物分子的识别,结合数字胶体增强拉曼光谱技术,实现了具有可重复性的低浓度药物分子的定量检测,灵敏度可达纳摩尔水平。此外,该技术采用的预处理方法简单、仪器成本低,操作便捷,有利于床旁的实时药效监测和个性化药物治疗。该快速、准确、灵敏的生物正交药物分子定量技术的提出有望在基础研究和临床监测中得到广泛应用。
关于本文
上海交通大学生物医学工程学院博士生毕心缘、硕士贺志成为本文的共同第一作者。上海交通大学生物医学工程学院叶坚教授为本文的通讯作者。该研究工作得到了国家自然科学基金委、上海市妇科肿瘤重点实验室、上海交通大学的支持。
叶坚教授课题组主页:http://www.yelab.sjtu.edu.cn
全文链接:https://pubs.rsc.org/en/Content/ArticleLanding/2024/SC/D4SC02553A